膜片鉗操作實驗
實驗原理
膜片鉗技術是一種通過玻璃微電極與細胞膜表面形成千兆歐姆以上高阻封接,從而將電極尖端所接觸的一小片細胞膜在電學上與其周圍區域隔離的技術。
該方法能夠在電壓固定的條件下,直接測量該膜片上離子通道產生的pA級離子電流。其測量回路的核心是場效應管運算放大器構成的I-V轉換器。該放大器正負輸入端子保持等電位,通過在正輸入端施加指令電壓,可使負輸入端與封接膜片均被鉗制在同一電位。當電極與細胞膜之間形成超過10GΩ的封接時,漏電流極小,流經膜片的電流可幾乎全部作為膜片電極電流(Ip)被記錄和測量。
實驗步驟
運用膜片鉗進行膜離子通道特性的研究,是一項艱辛、細致、繁雜的工作,要求較高的技術水平和實驗條件作保證,現在大致介紹一下膜片鉗實驗的過程,粗略地包括以下幾個方面。
1. 標本制備 根據研究目的的不同,可采用不同的細胞組織。對所采用的細胞,必須滿足實驗要求,一般多采用酶解分離法,也可采用細胞培養法。
2. 電極制備 合格的膜片微電極是成功封接細胞膜的基本條件。要成功的封接細胞膜需要兩方面的因素保證,一是設法造成干凈的細胞膜表面,二是制成合格的電極。首先要選擇適當的玻璃毛細管,其材料可使用軟質玻璃(蘇打玻璃、電石玻璃)或硬質玻璃(硼硅玻璃、鋁硅玻璃、石英玻璃)。膜片微電極是將玻璃毛細管用電極拉制儀拉制而成的,制作分三步進行:
第一步是分兩次拉制,第一次拉長7~10mm,直徑小于200um,在此基礎上進行第二次拉制,最終使尖端的直徑為1~2um,兩步拉制的目的主要是使電極前端的錐度變大,狹窄部長度縮短,因此可降低電極的串聯電阻,也可減少全細胞記錄時的電極液透析時間。由于膜片微電極最忌沾染灰塵和臟物,更忌觸碰尖端附近部位,所以一般要求在使用前制作。
第二步是在電極前端涂以硅酮樹脂(sylgard),其目的是為了降低電極與灌流液之間的電容,并形成一個親水界面。經此處理后,上述電容可由6~8pF減少到1pF以下。硅酮樹脂對形成Giga的seals無影響,但可減少本底噪音,對單通道記錄很重要。在進行全細胞記錄時,不用硅酮樹脂也可以得到滿意的效果,通常微電極在涂抹硅酮樹脂后再進行拋光,但最好是在涂抹后一小時內拋光,否則很難改變電極尖端的形狀。
第三步是拋光,將電極固定于顯微鏡工作臺上,在鏡下將尖端靠近加熱絲,當通電加熱時,可見電極尖端微微回縮,此時電極變得光滑,且尖端的雜質燒去,得到較干凈的表面。從而有利于和細胞膜緊密封接,并在封接后更易保持穩定。
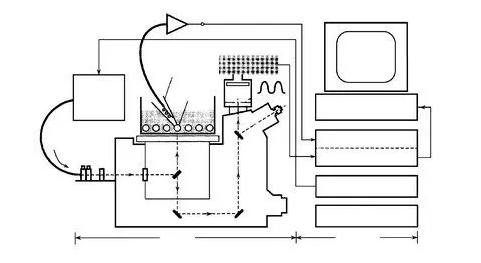
3.膜片鉗實驗系統 根據不同的電生理實驗要求,可以組建不同的實驗系統,但有若干共同的基本部件,包括機械部分(防震工作臺、屏蔽罩、儀器設備架)、光學部分(顯微鏡、視頻監視器、單色光系統)、電子部件(膜片鉗放大器、刺激器、數據采集的設備、計算機系統)和微操縱器。
4. 進行實驗,記錄和分析數據 準備工作就緒后即可進行實驗操作,數據記錄和分析。這里主要介紹高阻封接的形成。