【技術速遞】什么是膜片鉗技術?
1.膜片鉗技術的開創(chuàng) Initiate
膜片鉗實驗(Patch-clamp recording)是現(xiàn)代電生理學中一項革命性的技術,由Erwin Neher和Bert Sakmann于20世紀70年代末開創(chuàng)。 Erwin Neher和Bert Sakmann經(jīng)過13年的辛苦探索,終于在電壓鉗技術的基礎上,首次在青蛙肌細胞上用雙電極鉗制膜電位的同時,記錄到ACh激活的單通道離子電流,從而發(fā)展出膜片鉗技術,證明了離子通道的存在。Erwin Neher和Bert Sakmann榮獲1991年諾貝爾生理學或醫(yī)學獎。

圖1 Erwin Neher 德國,1944年-

圖2 Bert Sakmann 德國,1942年-
2.膜片鉗技術的原理 Principle
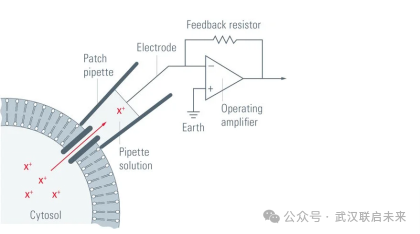
圖1 膜片鉗記錄的一般原理
膜片鉗技術的核心目標是在單個細胞乃至亞細胞水平上,在以前所未有的精度上,記錄離子通道的電流活動。
其基本原理是利用一個尖端直徑約為1-2微米的玻璃微電極(pipette),通過施加負壓與細胞膜形成一種電阻高達10^9歐姆以上的高阻封接(gigaohm seal)。這種封接在電學上將電極尖端下的一小塊細胞膜(稱為“膜片”)與細胞其余部分及外部溶液完全隔離,從而極大地降低了背景漏電流和熱噪聲,使得記錄單個離子通道開閉所產(chǎn)生的皮安級微弱電流成為可能。
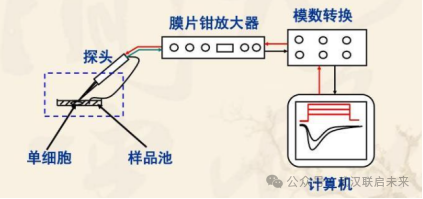
圖2 膜片鉗記錄儀器使用一般原理
3.四種記錄方法 Recording method
膜片鉗技術的強大之處在于其多種靈活的記錄構型,每種構型都為解答特定的生物學問題而設計。
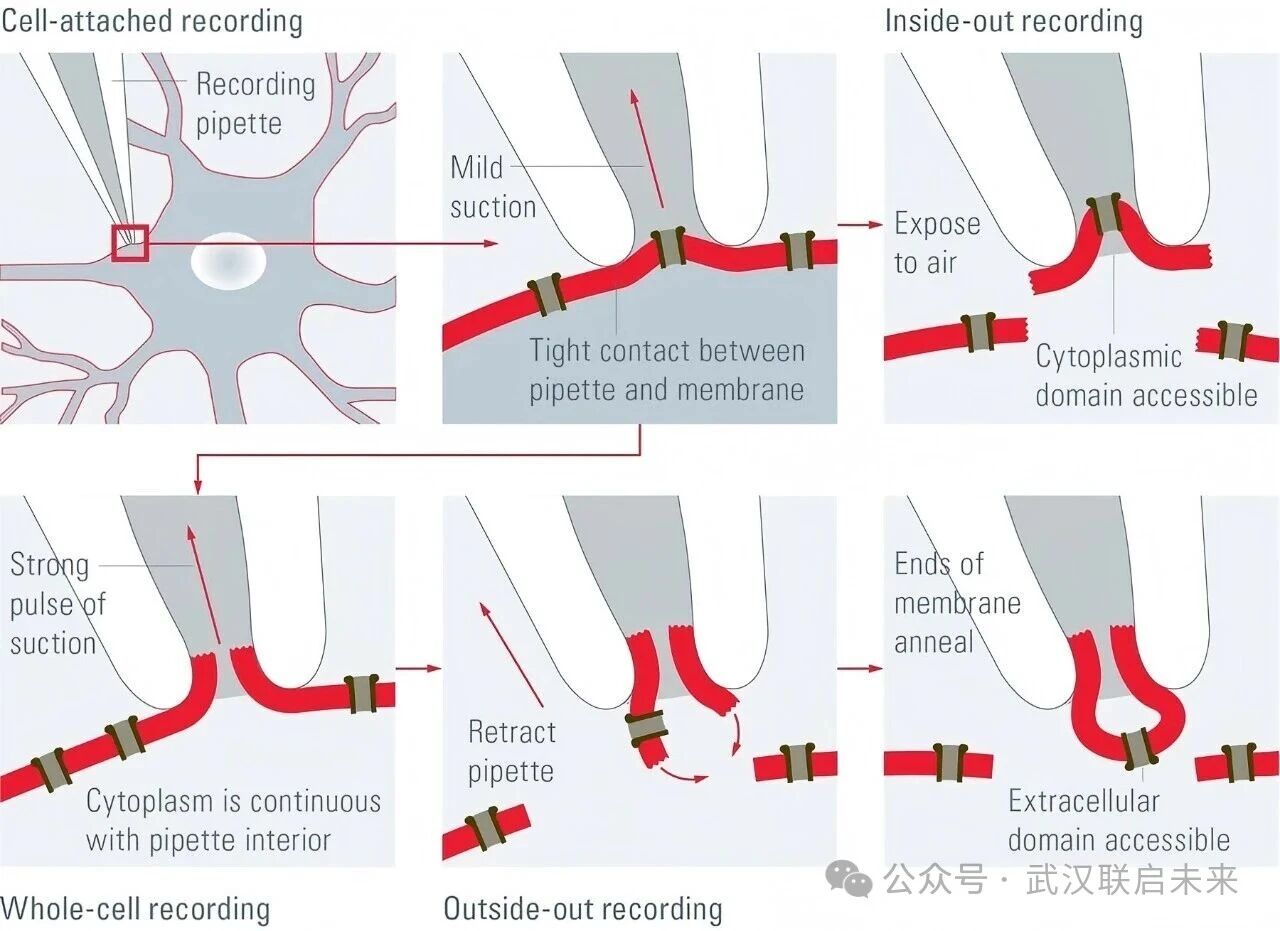
圖3 膜片鉗技術的四種記錄方法
最基礎的模式是細胞貼附式(cell-attached patch),在此模式下,電極與細胞膜形成吉歐姆封接,但細胞膜保持完整。這使得研究者能夠觀察膜片內(nèi)一個或少數(shù)幾個離子通道在其天然細胞質(zhì)環(huán)境中的活動,而不會干擾細胞內(nèi)部的信號分子。
當需要研究整個細胞的電活動時,則采用全細胞式(whole-cell recording)。在細胞貼附模式的基礎上,通過施加更強的負壓或短暫的電壓脈沖來破壞電極尖端下的膜片,從而建立電極內(nèi)液與細胞質(zhì)之間的直接電學和擴散通路。全細胞模式可以記錄流經(jīng)整個細胞膜的所有離子通道的總和電流,是研究動作電位、突觸傳遞等細胞整體電生理特性的主要手段。
然而,全細胞模式的一個顯著缺點是會導致細胞質(zhì)透析,即細胞內(nèi)的關鍵第二信使(如ATP、GTP、Ca2?)會被電極內(nèi)液稀釋或沖走,從而導致依賴這些分子的信號通路功能衰減。為克服此問題,研究人員創(chuàng)新了穿孔膜片鉗(perforated-patch)技術。
此外,還有兩種游離膜片模式:內(nèi)面向外式(inside-out)和外面向外式(outside-out)。前者通過將電極從細胞上提拉,使膜片的細胞質(zhì)側(cè)暴露于浴液中,便于精確控制和灌流細胞內(nèi)調(diào)控因子;后者則使膜片的細胞外側(cè)暴露于浴液,常用于研究配體門控通道或進行單通道動力學分析。
4.兩種操作模式 Operation mode
在操作模式上,膜片鉗系統(tǒng)主要工作于電壓鉗(voltage-clamp)和電流鉗(current-clamp)兩種狀態(tài)。
電壓鉗模式通過負反饋放大器將細胞膜電位精確地鉗制在研究者設定的指令電位上,并實時測量為維持該電位所需注入的電流。由于這個注入電流與流經(jīng)細胞膜離子通道的凈電流大小相等、方向相反,因此可以直接反映離子通道的活動。這是研究電壓門控或配體門控離子通道電導、選擇性、激活/失活動力學等生物物理特性的黃金標準。
相比之下,電流鉗模式則是向細胞注入一個已知的電流,并記錄由此引發(fā)的膜電位的自然變化。這種模式主要用于觀察神經(jīng)元的動作電位發(fā)放模式、靜息膜電位以及突觸后電位等生理事件。
5.膜片鉗技術的應用 Application
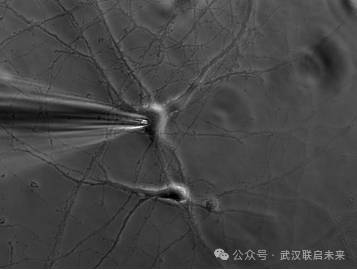
圖4 微電極貼附到培養(yǎng)小鼠海馬神經(jīng)元細胞膜的相差圖像。
圖片取自徠卡官網(wǎng) 由德國波鴻魯爾大學的Ainhara Aguado博士提供。
自問世以來,膜片鉗技術已成為生命科學研究不可或缺的基石工具。它不僅徹底改變了我們對離子通道這一“分子機器”的理解,還在多個領域發(fā)揮著核心作用。
在神經(jīng)科學中,它是解析突觸傳遞機制、繪制神經(jīng)環(huán)路連接、研究學習記憶的細胞基礎的關鍵手段。
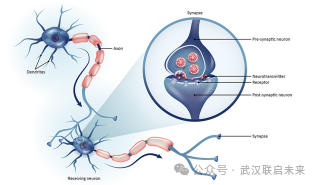
圖5 神經(jīng)軸突和突觸示意圖 在心臟電生理學和藥物安全藥理學中,膜片鉗被廣泛用于評估新藥候選物對心臟離子通道(如hERG鉀通道)的潛在致心律失常風險,是臨床前心臟安全性評價的“金標準”。
在疾病機制研究方面,它被用于診斷和表征由離子通道基因突變引起的“通道病”,如囊性纖維化、長QT綜合征和某些類型的癲癇。
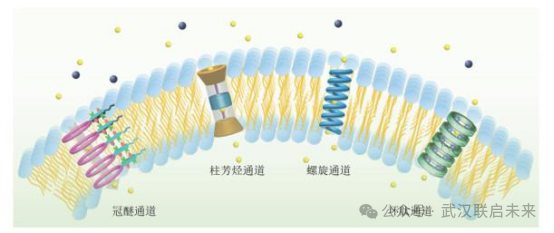
圖6 人工跨膜離子傳輸通道示意圖
隨著技術的發(fā)展,膜片鉗也正朝著自動化和高通量的方向演進。例如,基于微流控芯片的平面膜片鉗(planar patch-clamp)平臺,通過在芯片上集成微孔和電極,能夠?qū)崿F(xiàn)對多個細胞的并行記錄,顯著提高了藥物篩選的效率。
6.相關實驗儀器 Complementarity
顯微操作系統(tǒng) 分辨率的顯微鏡(通常配備微分干涉差DIC或霍夫曼調(diào)制對比HMC光學系統(tǒng))用于可視化。微操縱器則用于精確控制電極在三維空間中的移動,其步進精度需達到納米級別,以確保電極能輕柔、準確地接觸目標細胞膜并形成高阻封接。
玻璃微電極及其制備設備 微電極通常由硼硅酸鹽玻璃毛細管經(jīng)微電極拉制儀(Micropipette Puller)拉制而成,再通過微鍛儀(Microforge)進行拋光,以獲得光滑、尺寸均一的尖端。電極的物理特性(如尖端直徑、錐度、電阻)對封接成功率和記錄質(zhì)量有決定性影響。
膜片鉗放大器 主要功能是在電壓鉗模式下將微弱的皮安級離子通道電流轉(zhuǎn)換為可測量的電壓信號,同時在電流鉗模式下精確注入設定的電流并記錄膜電位變化。
振動隔離與電磁屏蔽系統(tǒng) 實驗臺必須置于氣浮式防震臺上,并放置在法拉第籠內(nèi),以有效隔絕地面振動和環(huán)境電磁噪聲。
水平拉制儀 HL-1000 水平拉制儀具有編制不同拉動程序的能力,可以方便地在一個儀器上拉制各種類型的玻璃微電極。



參考文獻: 【1】Nagarah, J. M., Paek, E., Luo, Y., Wang, P., Hwang, G. S., & Heath, J. R. (2010). Batch Fabrication of High‐Performance Planar Patch‐Clamp Devices in Quartz. Advanced Materials, 22(41), 4622–4627. 【2】Xu, B., Ye, W., Zhang, Y., Shi, J., Chan, C., Yao, X., & Yang, M. (2014). A hydrophilic polymer based microfluidic system with planar patch clamp electrode array for electrophysiological measurement from cells. Biosensors and Bioelectronics, 53, 187–192.